33.02 Все темы ("Без спойлеров")
Ошибка.
Попробуйте повторить позже
При сгорании 9 г органического вещества получили 13,2 г углекислого газа и 5,4 г воды. Известно, что это вещество не взаимодействует с карбонатом кальция, но реагирует с водным раствором гидроксида натрия. Напишите уравнение реакции данного вещества с водным раствором гидроксида натрия.
Источники:
1. Общая схема горения органического вещества:
Орг.вещество + O2 → CO2 + Н2О
Из условия задачи нам известны масса образовавшегося углекислого газа и масса выделившейся воды. Найдем их количества вещества:
n(СO2) = m(СO2) / M(СO2) = 13,2 / 44 = 0,3 моль
n(H2O) = m(H2O) / M(H2O) = 5,4 / 18 = 0,3 моль
2. Теперь проанализируем состав каждого выделившегося вещества:
СO2 - углекислый газ, состоит из одного атома углерода и двух атомов кислорода.
Атомы углерода в исходных веществах есть только в неизвестном органическом соединении, а в продуктах - только в углекислом газе. Следовательно, все атомы углерода, которые были в органическом соединении, "перешли" в углекислый газ.
Поэтому мы делаем вывод, что количество атомов углерода органического соединения численно равно количеству атомов углерода углекислого газа: При этом в одной молекуле углекислого газа есть только один атом углерода. Это означает, что количество атомов углерода в углекислом газе равно количеству вещества углекислого газа.
n(С) = n(CO2) = 0,3 моль
Отсюда масса атомов углерода в составе органического вещества:
m(С) = n(С) * M(С) = 0,3 * 12 = 3,6 г
H2O - вода, состоит из двух атомов водорода и одного атома кислорода.
Атомы водорода в исходных веществах есть только в неизвестном органическом соединении, а в продуктах - только в воде. Следовательно, все атомы водорода, которые были в органическом соединении, "перешли" в воду.
Поэтому мы делаем вывод, что количество атомов водорода органического соединения численно равно количеству атомов водорода в воде. При этом в одной молекуле воды есть два атома водорода. Это означает, что количество атомов водорода в два раза больше, чем количество вещества воды.
n(H) = 2 * n(H2O) = 0,6 моль
Отсюда масса атомов водорода:
m(H) = n(H) * M(H) = 0,6 * 1 = 0,6 г
3. Масса органического вещества по условию равна 9 г. Сложим вычисленные массы атомов углерода и водорода:
m(С) + m(H) = 3,6 + 0,6 = 4,2 г
Так как сумма масс атомов не равна массе органического вещества, значит в составе соединения есть атомы другого элемента.
Предположим, что в составе органического вещества содержится кислород.
Масса атомов кислорода в соединении равна разности массы всего вещества и суммы масс атомов углерода и водорода:
m(O) = m(Орг.вещества) - (m(C) + m(H)) = 9 - 4,2 = 4,8 г
Отсюда количество вещества атомов кислорода:
n(O) = m(O) / M(O) = 4,8 / 16 = 0,3 моль
4. Зная количество молей атомов вещества, можем определить их соотношение в органическом веществе:
n(С) : n(H) : n(O) = (0,3 : 0,6 : 0,3) | 0,3 = 1 : 2 : 1
Простейшая формула: CH2O. такой формуле может соответствовать формальдегид, однако он не подходит под описанные в задаче свойства (вещество должно прореагировать с водным раствором щелочи), поэтому удвоим количество атомов, получим: C2H4O2. Это формула соответствует общей формуле сложных эфиров и предельных карбоновых кислот - CnH2nO2. Но так как по условию: вещество не взаимодействует с карбонатом кальция, являться кислотой оно не может. Органическое вещество является сложным эфиром - метилформиатом 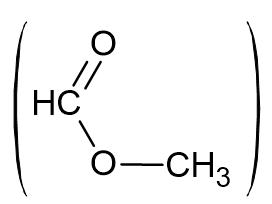 .
.
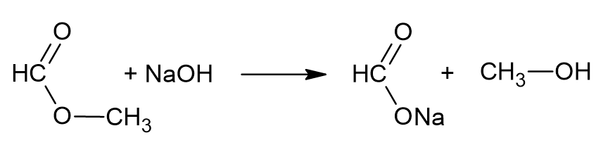
5. Напишем уравнение реакции данного вещества с водным раствором гидроксида натрия.
Специальные программы

Программа
лояльности v2.0
Приглашай друзей в Школково и получай вознаграждение до 10%!
Крути рулетку
и выигрывай призы!
Крути рулетку и покупай курсы со скидкой, которая привязывается к вашему аккаунту.

Бесплатное онлайн-обучение
Для школьников из приграничных территорий России, проживающих в ДНР, ЛНР, Херсонской, Запорожской, Белгородской, Курской, Брянской областях и Крыму.

Налоговые вычеты
Узнай, как получить налоговый вычет при оплате обучения в «Школково».
Специальное предложение
для учителей
Бесплатный доступ к любому курсу подготовки к ЕГЭ, ОГЭ и олимпиадам от «Школково». Мы с вами делаем общее и важное дело, а потому для нас очень значимо быть чем-то полезными для учителей по всей России!

Вернём деньги за курс
за твою сотку на ЕГЭ
Сдать экзамен на сотку и получить обратно деньги за подготовку теперь вполне реально!




